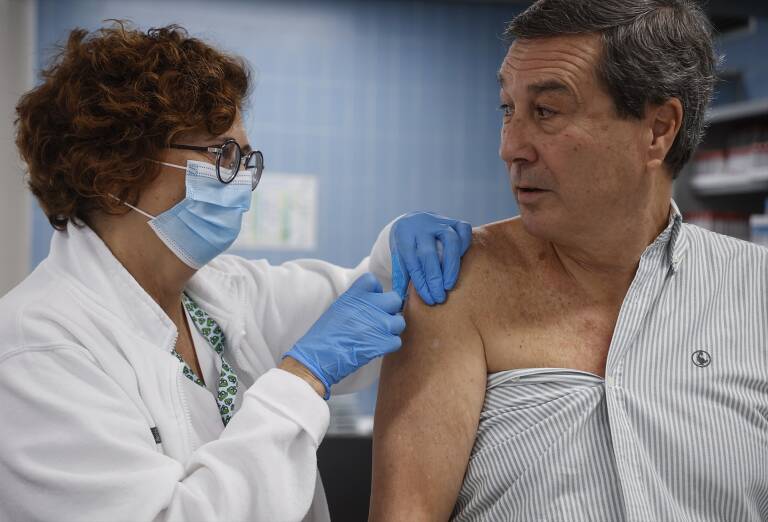
Esta también está indicada para la inmunización activa de mayores de 60 años
La EMA da su visto bueno a la primera vacuna contra el VRS para lactantes de hasta 6 meses

 Foto: EUROPA PRESS
Foto: EUROPA PRESSVALÈNCIA (EP). La Agencia Europea de Medicamentos (EMA, por sus siglas en inglés) ha recomendado la concesión de una autorización de comercialización en la Unión Europea (UE) para 'Abrysvo', una vacuna que protege contra la enfermedad causada por el virus respiratorio sincitial (VRS).
'Abrysvo' es la primera vacuna contra el VRS indicada para la inmunización pasiva de lactantes desde el nacimiento hasta los 6 meses de edad tras la administración de la vacuna a la madre durante el embarazo. Esta vacuna también está indicada para la inmunización activa de mayores de 60 años.
El VRS es un virus respiratorio común que suele causar síntomas leves parecidos a los del resfriado, pero puede tener consecuencias graves en niños y adultos mayores. De hecho, en los niños el VRS es una de las principales causas de hospitalización pediátrica en Europa. Puede causar bronquiolitis y neumonía y provocar una insuficiencia respiratoria mortal.
La infección por VRS también puede ser grave para los adultos a partir de 50 años, ya que puede causar una infección respiratoria aguda, una enfermedad similar a la gripe o una neumonía adquirida en la comunidad.
'Abrysvo' es una vacuna bivalente compuesta por dos glicoproteínas de superficie de fusión recombinantes del VRS seleccionadas para optimizar la protección frente a las cepas A y B del VRS. Estas proteínas son esenciales para que el VRS infecte el organismo y son también las dianas principales de los anticuerpos generados para combatir la infección.
Cuando una persona recibe la vacuna, su sistema inmunitario genera anticuerpos específicos y células T (células del sistema inmunitario) que ayudan a prevenir la infección por VRS. En el caso de las personas embarazadas, los anticuerpos neutralizantes atraviesan la placenta, proporcionando a los lactantes protección hasta 6 meses después del nacimiento.
El dictamen del Comité de Medicamentos de Uso Humano de la EMA se basa en los datos de dos estudios pivotales aleatorizados y controlados con placebo.
En un estudio, se administró 'Abrysvo' a 3.695 personas con un embarazo de entre 24 y 36 semanas, mientras que 3.697 recibieron un placebo (inyección simulada). La evaluación demostró que la vacuna era eficaz para reducir tanto las enfermedades graves de las vías respiratorias inferiores con asistencia médica como las enfermedades de las vías respiratorias inferiores con asistencia médica que se producían en los 180 días siguientes al nacimiento.
En el otro estudio, se administró la vacuna a 18.488 adultos mayores de 60 años, mientras que 18.479 recibieron un placebo. Los resultados del estudio demostraron la eficacia de 'Abrysvo' en la reducción de las enfermedades de las vías respiratorias inferiores asociadas al VRS con 2 (o más) síntomas y con 3 (o más) síntomas.
Los efectos secundarios más frecuentes notificados en individuos de entre 24 y 36 semanas de gestación fueron dolor en el lugar de vacunación, dolor de cabeza y dolor muscular. En personas de 60 años o más, el efecto secundario notificado con más frecuencia fue dolor en el lugar de vacunación.
El dictamen de la EMA se enviará ahora a la Comisión Europea para que adopte una decisión sobre la autorización de comercialización en toda la UE. Una vez concedida, las decisiones sobre el precio y el reembolso se tomarán a nivel de cada Estado miembro, teniendo en cuenta el papel/uso potencial de este medicamento en el contexto del sistema sanitario nacional de cada país.